Biologie
úvod
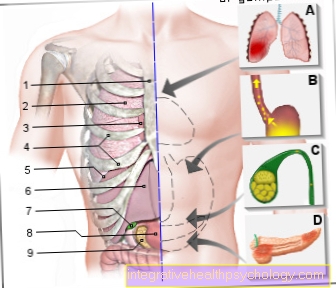
Imunitní systém je nezbytný pro přežití každé lidské bytosti. V průběhu evoluce se to u lidí vyvinulo v tzv. Adaptivní imunitní systém. To nám dává příležitost reagovat odlišněji a účinněji na bakterie a viry. Imunitní systém nás chrání. Pomáhá nám lépe přežít bitvu se zánětem. Existuje mnoho různých typů modulátorů zánětu. Například takzvaný faktor nekrózy nádorů alfa, který je zkráceně TNF-a. Spolu s dalšími faktory to zajišťuje, že zánětlivé a nádorové buňky jsou eliminovány dříve, než mohou vyvolat onemocnění.

Tito „tělesní strážci“ našeho těla se však mohou stát také „zločinci“. Protože někdy se náš imunitní systém obrací proti nám. V těchto případech se vyvinou autoimunitní onemocnění, která je obtížně léčitelná léky. Zde přichází biologie. Biologie se také nazývají biofarmaka nebo biofarmaka. Jedná se o léčiva, která se vyrábějí v geneticky modifikovaných organismech pomocí různých biotechnologických prostředků. Příklady těchto léčiv jsou takzvané „monoklonální protilátky“ nebo tzv. „Fúzní proteiny“. Inhibitory TNF-a, mezi nimi antagonisty receptoru TNF-alfa, patří do této skupiny léčiv.
Známou biologickou látkou je adalimumab, známý také pod obchodním názvem Humira.
Indikace
Antagonisté receptoru TNF-a se používají při zánětlivých chronických autoimunitních onemocněních. To znamená, že jsou indikovány na všechna onemocnění, kde vlastní imunitní systém těla bojuje proti tělu, místo aby o něj bojoval. V tomto procesu hraje TNF-a často hlavní roli. Zajišťuje, že určité buňky se začnou chovat jako tzv. Vychytávací buňky (makrofágy), a tak ničí tkáň, kosti, chrupavku a v závislosti na nemoci i další tělesné buňky.
Specifické indikace jsou například revmatoidní artritida, tzv. Juvenilní idiopatická artritida, psoriatická artritida, plaková psoriáza, ankylozující spondylitida, Crohnova choroba nebo ulcerózní kolitida. Biologická léčiva, jako jsou antagonisté receptoru TNF-a, se používají, pokud žádná jiná léčiva nepomáhají s uvedenými nemocemi nebo nezpůsobují příliš mnoho vedlejších účinků.
Biologie pro ankylozující spondylitidu
Bechterewova nemoc je zánětlivé, chronické autoimunitní onemocnění. Patří do revmatické skupiny forem. Je to jedna z tzv. Spondylartritid. Při Bechterewově nemoci je vlastní imunitní systém těla namířen proti kostním a chrupavkovým buňkám v pánevní a zadní oblasti a ničí je. To může vést k bolesti kloubů a deformacím v odpovídajících částech těla. Za určitých okolností lze také použít antagonisty receptoru TNF-a. Inhibují messengerovou látku TNF-a. Protože tato messengerová látka hraje hlavní roli v zánětlivém procesu, proces nemoci je blokován inhibicí TNF-a. To může zmírnit příznaky a zpomalit progresi onemocnění.
Přečtěte si více o tomto tématu na: Terapie ankylozující spondylitidy
Biologie pro lupénku
Hovorová psoriáza je v technickém žargonu známa jako plaková psoriáza. Projevuje se jako silné odlupování kůže svěděním a pálivou bolestí. Může se vyskytnout v různých stupních závažnosti. V případě střední až těžké závažnosti se někdy používají antagonisty receptoru TNF-a.
Jeden mluví o této závažnosti nemoci, když je postiženo více než 10% povrchu kůže nebo když se kožní změny projeví ve zvláště viditelných částech těla, jako jsou ruce nebo obličej. Velmi vysoká úroveň utrpení ze strany pacienta je také kritériem pro klasifikaci střední až těžké psoriázy. V některých případech může být biologie již použita, aniž by došlo k selhání všech ostatních účinných látek nebo k prokázání vedlejších účinků. Antagonisté receptoru TNF-a mohou potlačit zánětlivé reakce v místě, kde vznikají, a tak zlepšit kvalitu života postiženého pacienta.
Kromě toho lze do jisté míry zabránit sekundárním onemocněním, která mohou být důsledkem psoriázy, jako je deprese.
Přečtěte si více o tomto tématu na: Psoriáza nebo léčba lupénky
Biologie pro ulcerativní kolitidu
Ulcerózní kolitida je charakterizována silnými zánětlivými, chronickými, přerušovanými procesy střevní sliznice a základní vrstvou pojivové tkáně. V těžkých případech se tvoří vředy. Na rozdíl od Crohnovy choroby je tlusté střevo téměř výlučně zasaženo. Také u tohoto typu autoimunitního onemocnění mohou antagonisté receptoru TNF-a pozitivně ovlivnit průběh onemocnění. Pro léčbu ulcerózní kolitidy bylo nyní schváleno mnoho různých biologických látek.
Přečtěte si více o tomto tématu na: Terapie ulcerativní kolitidy
Biologie Crohnovy choroby
Crohnova nemoc je chronické zánětlivé autoimunitní onemocnění. Vlastní obranný systém těla je namířen proti buňkám zažívacího traktu. To může ovlivnit celý trávicí systém od ústní dutiny po konečník. Zde hraje TNF-a roli v tom, že zajišťuje výskyt zánětlivých procesů a ničení buněk. Inhibitory TNF-a proto mohou také potlačovat procesy onemocnění v souvislosti s Crohnovou chorobou a částečně zabránit následnému poškození.
Přečtěte si více o tomto tématu na: Terapie Crohnovy choroby
Biologie pro revmatismus
Mnoho nemocí je revmatických. Když je revmatismus používán hovorově, je to obvykle revmatoidní artritida. Jedná se o chronické zánětlivé autoimunitní onemocnění, při kterém imunitní buňky ničí chrupavkové a kostní buňky. Bolest kloubů a otoky. K tomu často dochází v oblasti metatarsofalangálních kloubů prstů a prstů na nohou. Často se vyskytuje typická ranní ztuhlost. I zde hraje hlavní roli modulátor zánětu TNF-a. Antagonisté receptoru TNF-a mohou být použity při léčbě revmatoidů, pokud jiná opatření selžou.
Přečtěte si více o tomto tématu na: Terapie revmatoidní artritidy
Účinná látka / účinek
Většina biologik jsou proteiny. Existují různé generace biologických látek, a tedy také inhibitorů TNF-a. Generace se liší od výroby.
Konec názvu ukazuje, kolik myšího proteinu je stále přítomno v aktivních složkách. S koncovým –omab je to 100%, s koncovým –ximab je stále 25% myší protein, s koncovým - 5–10% je stále k dispozici a s koncovým –umab vůbec. To hraje roli v snášenlivosti léků.
Inhibitory TNF-a mohou navíc fungovat různými způsoby. Mohou zachytit TNF-a, a tím mu zabránit v navázání na jeho receptor. V důsledku toho nedochází k určitým procesům v buňce, které by vedly k destruktivní imunitní reakci.Další možností je, že inhibitor TNF-a blokuje vazebné místo TNF-a k receptoru. Lék pak působí jako tzv. Antagonista. Je také možné, že inhibitory TNF-a působí jako tzv. Fúzní proteiny. Nazývají se také návnadové receptory. Falešné receptory jsou receptory, které vážou ligandy, ale nevysílají signály. TNF-a návnadové receptory jsou rozpustné receptory, které zachycují TNF-a předtím, než dosáhne svého původního cíle. Výsledkem je, že již neexistuje žádný signál a růst destruktivních imunitních buněk je zpomalen.
Enbrel®
Účinná látka Etanercept je přítomna v komerčním přípravku Enbrel®. Je to takzvaný návnadový receptor nebo fúzní protein. Enbrel® se používá zejména při revmatické artritidě, juvenilní chronické artritidě, psoriatické artritidě a tzv. Spondylartritidě. Psoriatická artritida je zvláštní forma psoriázy, která je spojena s bolestí kloubů. Enbrel® působí jako inhibitor TNF-a u těchto onemocnění, jakož i u některých jiných autoimunitních onemocnění. Enbrel® však není účinný při Crohnově chorobě. Zpravidla se podává subkutánně jednou týdně s 50 mg nebo dvakrát týdně s 25 mg.
Přečtěte si více o tomto tématu na: Enbrel®
Remicade®
Účinnou složku infliximab lze nalézt například v komerčním přípravku Remicade®. Infliximab je chimérická monoklonální protilátka, která blokuje aktivitu TNF-a. Protože se jedná o chimérickou monoklonální protilátku, je hlavní páteř lidská a vazebná místa pro antigen (25%) jsou myší protein. To znamená, že účinnost je vyšší než u tzv. Myších monoklonálních protilátek, které se skládají ze 100% myšího proteinu, a nižší ve srovnání s humanizovanými (5-10% myší protein) nebo lidskými monoklonálními protilátkami (0% myší protein). Riziko alergií a intolerance je tedy nižší než u myších monoklonálních protilátek a vyšší než u humanizovaných nebo lidských protilátek. Remicade® se používá pro revmatoidní artritidu, psoriatickou artritidu, ankylozující spondylitidu a jiná autoimunitní onemocnění. Na rozdíl od etanerceptu je účinná látka infliximab účinná také u Crohnovy choroby. Dávka je 3-5 mg na kg tělesné hmotnosti v závislosti na onemocnění.
dávkování
Protože jsou bilogiky obvykle proteiny, musí být podávány parenterálně (infuzí). Orální požití není možné, protože tělo by ho pak strávilo a aktivní složky si nemohly vyvinout svůj účinek. Dávka závisí na aktivní složce a na přítomném onemocnění. Dávka je obvykle v jednociferném až dvoumístném miligramovém rozmezí a podává se 1-2krát týdně.
cena
Náklady na biologiku jsou velmi vysoké. Proto se většinou používají pouze jako poslední možnost. To znamená, že pokud jsou všechny další aktivní složky, které jsou indikovány pro příslušná onemocnění, neúspěšné. Dvě stříkačky zpravidla stojí přibližně 1600 EUR měsíčně.
Vedlejší efekty
V rámci specializované léčby a pozorování jsou blokátory TNF-a relativně dobře tolerované a bezpečné léky. Stejně jako u jakéhokoli léku se však mohou objevit vedlejší účinky. Vedlejší účinky lze rozdělit na účinky související s aplikací a účinky související s interferencí s imunitním systémem. Protože biologika musí být podávána parenterálně (jako infuze), mohou se teoreticky vyskytnout infuzní reakce. Ve srovnání s jinými biologiemi se to stává častěji u účinné látky infliximab. Ale s odbornou léčbou, tyto typy vedlejších účinků mohou být obvykle dobře kontrolovány. Pokud jsou Biologikas podávány subkutánně (pod kůži), mohou být vyvolány lokální kožní reakce. Přerušení léčby však bylo dosud velmi zřídka nutné.
Vedlejší účinky, které se objevují v důsledku interference s imunitním systémem, jsou založeny na dalším potlačení fyziologických procesů v našem těle. Poselská látka TNF-a je ve skutečnosti důležitým modulátorem zánětu. I když je částečně namířen proti imunitnímu systému, má důležité úkoly týkající se imunitního systému. Pokud jsou tyto důležité funkce TNF-a léky trvale blokovány, může to vést k odpovídajícím vedlejším účinkům. Citlivost na infekce se může zvýšit a riziko rakoviny se může také zvýšit při dlouhodobém používání. Může dojít k poškození jater, ledvin a srdce. Inhibitory TNF-a mohou navíc reaktivovat inaktivní tuberkulózu a herpes zoster.
V závislosti na tom, která generace monoklonálních protilátek je, je riziko nesnášenlivosti a alergií vyšší nebo nižší. To znamená, že čím více myšího proteinu je stále přítomno v aktivní složce, tím větší je riziko alergií a intolerance. Kromě toho mohou nastat určité autoprotilátky. Léčba inhibitorem TNF-a málokdy vedla k tomu, co se nazývá lupus erythematosus. To se také snížilo, když byla biologická látka vysazena. Kromě toho byla popsána různá onemocnění a relapsy v souvislosti s roztroušenou sklerózou, jakož i zhoršení v případě výrazné srdeční nedostatečnosti.
interakce
Pokud se podají očkování živými vakcínami a současně inhibitory TNF-a, může to vyvolat onemocnění vakcinačním patogenem místo očkovacího účinku. Kromě toho lze pozorovat interakci při kombinaci dvou biologických léčiv. To bylo například pozorováno při současném podávání etanerceptu a anakinry v průběhu léčby revmatoidní artritidy. Účinek nebyl zlepšen, ale vedlejší účinky byly zesíleny. Vznikly vážné infekce a nedostatek určitých krvinek, takže se vyvinula tzv. Neutropenie.
Kdy by se neměla brát biologie?
Pokud existuje předchozí tuberkulóza, neměly by být použity žádné inhibitory TNF-a. To je bez ohledu na to, jak dlouho jste měli tuberkulózu. Důvodem je skutečnost, že inaktivované bakterie tuberkulózy jsou v těle stále přítomny i poté, co někdo trpí tuberkulózou. Tyto bakterie tuberkulózy jsou neaktivní, protože na ně dohlíží tzv. Makrofágy. Postarají se o to, aby bakterie nebyly znovu aktivní. Aby makrofágy mohly tuto úlohu plnit, potřebují TNF-a. Pokud již makrofágy kvůli účinku léku nejsou dostatečně dostupné, nemohou již vykonávat svůj úkol. Výsledkem je, že bakterie tuberkulózy se mohou znovu aktivovat a reaktivovat tuberkulózu.
Kromě toho je přítomnost hepatitidy B kontraindikací pro léčbu biologickým činidlem. Bylo zjištěno, že v tomto případě může léčba inhibitorem TNF-a reaktivovat herpes zoster. To se projevilo zvýšeným výskytem pásového oparu a planých neštovic u dospělých.
Byly však zjištěny rozdíly v různých aktivních složkách inhibitorů TNF-a. Nemoci se vyskytovaly častěji u pacientů léčených infliximabem, zatímco tyto vedlejší účinky nebylo možné při léčbě etanerceptem pozorovat. Úroveň rizika reaktivace korelovala s věkem u obou nemocí, s tzv. Komorbiditou (další onemocnění) as další léčbou glukokortikoidy, jako je kortizon.
Za účelem ochrany pacienta je však v současnosti případ, že léčba inhibitorem TNF-a není obecně povolena v případě předchozí tuberkulózy nebo hepatitidy B.
Biologie a alkohol - jsou kompatibilní?
Při léčbě biologickými látkami nemusíte dělat úplně bez alkoholu. Existují však zprávy o zkušenostech, ve kterých byly popsány nesnášenlivosti. Protože biologika ovlivňuje funkce ledvin a jater, je docela možné, že konzumace alkoholu může vést k akutní nesnášenlivosti. Kromě toho může dlouhodobá konzumace alkoholu v kombinaci s biologickými drogami zvyšovat riziko onemocnění jater a ledvin.
Náklady na léčbu
Náklady jsou velmi vysoké díky výrobnímu procesu a parenterální administraci. Inhibitory TNF-a stojí přibližně 40 000 až 50 000 EUR ročně. Jedna aplikace je alespoň v horním dvoumístném rozsahu. Kromě toho existují osobní náklady, náklady na předběžná vyšetření atd. Pokud by se odborník v praxi nebo na klinice měl rozhodnout, že léčba biologickým přípravkem je nejlepší formou terapie, musí k tomu uvést dobrý důvod. Může uhradit náklady zdravotní pojišťovně. Zpracování aplikace obvykle trvá několik týdnů. Jakmile je žádost zkontrolována, zpracována a schválena, uhradí náklady zdravotní pojišťovna. Může však omezit dobu převzetí. Závazek v oblasti nákladů je často zpočátku prováděn po dobu 3 měsíců. Poté je třeba podat novou žádost.
V roce 2016 byly oficiálně schváleny první tzv. Biosimilary pro léčbu revmatických chorob. Jak už název napovídá, jsou podobné Biologikům, ale nejsou stejné jako původní. Někteří autoři tvrdí, že jsou levnější alternativou k biologii. Je sporné, zda jejich účinek skutečně odpovídá účinku originálu. Zdravotní pojištění doufají, že ušetří miliardy nákladů. Ostatní odborníci jsou vůči odhadům skeptičtí. Dosud byly biosimilars používány pouze u přibližně 1–2% pacientů s revmatismem. Biosimilars jsou doporučeny Německou společností pro revmatologii. Nedoporučuje však přecházet z původního na náhradní produkt. Protože k tomu dosud neexistují žádné dlouhodobé studie, nemůže odborná společnost tímto způsobem uvítat změnu aktivních složek. Také nedoporučuje přijímat taková rozhodnutí pouze z důvodu nákladů. Kromě toho je příliš optimistická při posuzování úspor nákladů. V souhrnu lze říci, že zatím není možné odhadnout, jak bude používání biologie vypadat v budoucnosti, navzdory nákladům.